Teléfono: +86 576 8880 5030
Correo electrónico: sales@peekchina.com
Desde 2008 fabricante chino de estándares PEEK
Teléfono: +86 576 8880 5030
Correo electrónico: sales@peekchina.com
Desde 2008 fabricante chino de estándares PEEK


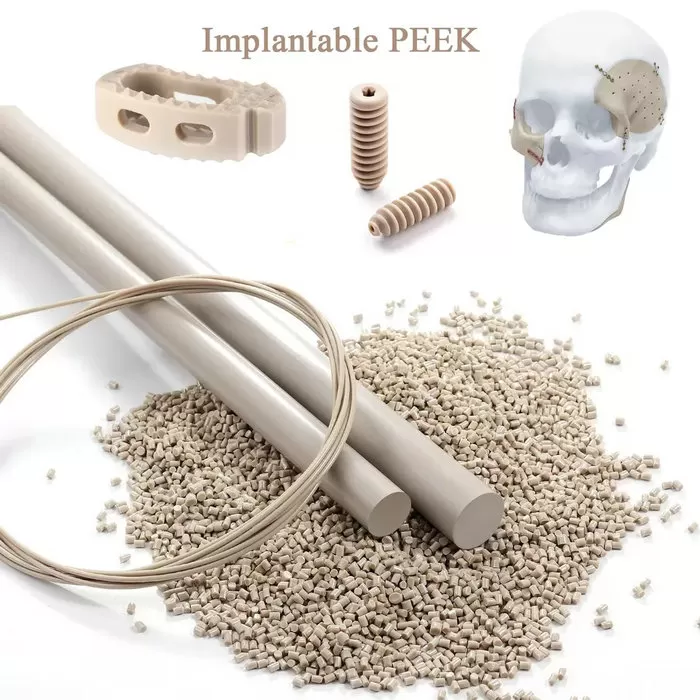

Guía de PEEK de grado implantable - PEEK para implantes médicos
El implante PEEK, o poliéterétercetona, es un material termoplástico de alto rendimiento ampliamente utilizado en la industria médica debido a sus propiedades excepcionales. El PEEK es reconocido por su biocompatibilidad, radiolucidez y resistencia, lo que lo convierte en una elección ideal para una variedad de aplicaciones médicas como implantes espinales, implantes dentales y dispositivos ortopédicos. En esta guía completa, exploraremos los beneficios del uso de implantes de PEEK en procedimientos médicos, incluyendo mejoras en los resultados para los pacientes, tiempos de cicatrización más rápidos y reducción del riesgo de complicaciones.
Diseñados para satisfacer los exigentes requisitos de los procedimientos quirúrgicos, nuestros polímeros PEEK exhiben una biocompatibilidad excepcional, lo que permite una implantación segura y confiable en el cuerpo humano. La resistencia mecánica de ARK-BioPEEK garantiza robustez y durabilidad, ofreciendo el soporte necesario para que los implantes quirúrgicos puedan resistir diversas tensiones fisiológicas.
Con la estabilidad térmica como característica clave, nuestros materiales PEEK mantienen su integridad estructural incluso en condiciones desafiantes, lo que permite un rendimiento y una estabilidad a largo plazo en el entorno del implante. La resistencia a la degradación y al desgaste de los materiales prolonga su vida útil, brindando confianza tanto a los profesionales de la salud como a los pacientes.
ARK-BioPEEK prioriza el bienestar y la seguridad de los pacientes, por eso nuestros polímeros PEEK se someten a rigurosas pruebas y validación para garantizar su idoneidad para aplicaciones de implantes quirúrgicos. Nuestro compromiso con la innovación nos impulsa a mejorar continuamente el rendimiento y las propiedades de nuestros materiales PEEK, asegurando que se mantengan a la vanguardia de las soluciones de implantes quirúrgicos.
Elija ARK-BioPEEK para sus necesidades de implantes quirúrgicos y experimente los beneficios de los materiales PEEK de próxima generación. Confíe en nuestra experiencia, confiabilidad y dedicación para ofrecer polímeros PEEK de alta calidad que redefinen los estándares de las aplicaciones de implantes quirúrgicos.
| Properties Information | ||||||
| Property | Reference Standard | Test Method | Unit | Specification | Result | |
| Physical Properties | Glass Transition | ASTM F2026 | ASTM D3418 | °C | 125-165 | 147 |
| Temperature, Tg | ||||||
| Melt Temperature, Tm | ASTM F2026 | ASTM D3418 | °C | 320-360 | 338 | |
| Recrystallization | ASTM F2026 | ASTM D3418 | °C | 260-320 | 289 | |
| Temperature, Tc | ||||||
| Viscosity | ASTM F2026 | ISO 11443 | Pa·s | 400-480 | 437 | |
| Infrared Spectrum | ASTM F2026 | ASTM F1579 | / | See Appendix X1 | See Appendix X2 | |
| Density | ASTM F2026 | ASTM D1505 | kg/m3 | 1280-1320 | 1294 | |
| Chemical Properties | Total Heavy Metals (Ag, As, Bi, Cd, Cu, Hg, Mo, Pb, Sb, and Sn), max | ASTM F2026 | US Pharmacopeia, | ppm | <100 | <10 |
| Test 233 | ||||||
| Mechanical Properties | Tensile Strength at Yield (zero slope), min | ASTM F2026 | ASTM D638, Type IV, 5.08 cm/min | MPa | 90 | 105 |
| Tensile Strength at Break, min | ASTM F2026 | ASTM D638, Type IV, 5.08 cm/min | MPa | 70 | 80 | |
| Elongation at Break, min | ASTM F2026 | ASTM D638, Type IV, 5.08 cm/min | % | 5 | 18 | |
| Flexural Strength, min | ASTM F2026 | ASTM D790 | MPa | 110 | 163 | |
| Flexural Modulus, min | ASTM F2026 | ASTM D790 | GPa | 3 | 4 | |
| Impact Strength, | ASTM F2026 | ISO 180 | kJ/m2 | 4 | 9 | |
| Notched Izod, min | ||||||
| Biological Properties | Genotoxicity | ISO 10993-3 | ISO 10993-3 | / | Negative | Negative |
| Animal Intracutaneous (Intradermal) Reactivity | ISO 10993-10 | ISO 10993-10 | / | ≤1 | 0 | |
| Skin Sensitization | ISO 10993-10 | ISO 10993-10 | / | ≤1 | 0 | |
| Acute Systemic Toxicity | ISO 10993-11 | ISO 10993-11 | / | No Acute Systemic Toxicity | No Acute Systemic Toxicity | |
| Subchronic Systemic Toxicity | ISO 10993-11 | ISO 10993-11 | / | No Subchronic Systemic Toxicity | No Subchronic Systemic Toxicity | |
| local Effects After Implantation | ISO 10993-6 | ISO10993-6 | / | No obvious difference between the test sample and the control sample | No obvious difference between the test sample and the control sample | |
| In Vitro Cytotoxicity | ISO 10993-5 | ISO10993-5 | / | ≤1 | 1 | |
| Evaluation of Haemolytic Properties | ISO 10993-4 | ISO10993-4 | % | <5 | 1 | |
| Material Mediated Pyrogens | ISO 10993-11 | ISO 10993-11 | / | No Pyrogenic Responses | No Pyrogenic Responses | |
| Extractables of The Material | ISO 10993-18 | ISO 10993-18 | μg/g | The contents of Phenyl Sulfone≤300 | The contents of Phenyl Sulfone<0.09 | |